Gestione dell'iponatremia ipotonica post-intervento neurochirurgico della regione ipotalamo-ipofisaria
Rita Indirli1,2, Emanuele Ferrante1
1SC Endocrinologia, Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico, Milano, Italia
2Dipartimento di Scienze Cliniche e di Comunità, Università degli Studi di Milano, Milano, Italia
Per corrispondenza:
Dr.ssa Rita Indirli
Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico, SC Endocrinologia
Via F. Sforza 35 – 20122 Milano (MI)
Tel. 02 5503 3481 – Mobile 340 5241761
[email protected]
Introduzione
L’iponatremia ipotonica può presentarsi dopo chirurgia ipotalamo-ipofisaria a causa del rilascio inappropriato di vasopressina (SIAD) che consegue al danno chirurgico o vascolare dell’ipotalamo, del peduncolo ipofisario e/o della neuroipofisi [1]. Può presentarsi isolatamente oppure nell’ambito di un deficit di vasopressina (AVP-D) bifasico o trifasico, a seconda dell’entità e della sede -distale o prossimale- del danno al corpo dei neuroni magnocellulari. La prevalenza riportata di questi disturbi è variabile: 8-25% per l’iponatremia isolata, 4-20% per l’AVP-D bifasico, e circa 1% per l’AVP-D trifasico. Sebbene alcuni studi avessero indicato che le dimensioni del tumore ipofisario e la malattia di Cushing si associassero ad un maggiore rischio di iponatremia, ad oggi non ci sono fattori predittivi certi di questa complicanza [1].
Presentazione clinica
La SIAD dopo chirurgia ipotalamo-ipofisaria ha generalmente una presentazione ritardata, comparendo tra la 4a e la 12a giornata (più frequentemente in 7a) [2]. Dal momento che, nel caso di un decorso post-operatorio non complicato, la dimissione è spesso programmata in 3-4a giornata, il paziente deve essere istruito a riconoscere i sintomi dell’iponatremia al domicilio, e può essere buona norma richiedere il dosaggio del sodio plasmatico in 6-7a giornata anche in un setting ambulatoriale [3]. La maggior parte dei pazienti infatti sviluppa un’iponatremia paucisintomatica, rendendo pertanto giustificato il monitoraggio della sodiemia. Tuttavia, data la riduzione acuta (<48 ore) dei livelli di sodio, ed in base alla sua entità, alcuni pazienti possono presentare sintomi moderati (cefalea, nausea, confusione mentale) o severi (vomito, distress respiratorio, convulsioni, sopore, coma) [4].
Diagnosi differenziale
L’iponatremia da SIAD deve essere differenziata da altre forme di iponatremia (Tabella 1), che possono richiedere trattamenti differenti e hanno in genere una presentazione più precoce rispetto alla SIAD (1-2^ giornata) [1, 5].
L’iposurrenalismo può associarsi a iponatremia euvolemica e può essere una complicanza della chirurgia ipotalamo-ipofisaria, soprattutto nella malattia di Cushing. Può presentarsi con astenia, anoressia, ipoglicemia, ipotensione ortostatica. In attesa della conferma diagnostica, è fondamentale la somministrazione di terapia glucocorticoide che in genere determina una rapida risoluzione dei sintomi e dell’iponatremia.
L’ipotiroidismo può determinare iposodiemia solo nelle forme severe, talvolta come conseguenza di un ipotiroidismo precedente misconosciuto o non adeguatamente trattato [1]. La terapia con levotiroxina permette una rapida risoluzione del quadro.
L’iponatremia può inoltre conseguire alla somministrazione intraoperatoria di fluidi ipotonici, ed in questo caso si risolve spontaneamente.
L’iperglicemia può determinare iponatremia ipertonica (da diluizione, essendo il glucosio un’osmole efficace) ed è un’evenienza da considerare nei pazienti con diabete preesistente, acromegalia o malattia di Cushing.
Infine, sebbene estremamente rara, una condizione che va differenziata dalla SIAD è la Cerebral Salt Wasting Syndrome (CSWS). Si tratta in questo caso di un’iponatremia ipovolemica conseguente alla natriuresi-diuresi indotta dal rilascio di peptide natriuretico cerebrale in pazienti in condizioni critiche (es. emorragia subaracnoidea). Le terapie per la SIAD sono inappropriate per la CSWS, la cui distinzione è quindi di fondamentale importanza (Tabella 1) [2].
Trattamento
Il trattamento maggiormente utilizzato per la correzione dell’iponatremia post-chirurgica è la restrizione idrica. Tuttavia, nei casi con iponatremia moderata (130-125 mEq/L) o severa (<125 mEq/L), soprattutto se sintomatica, possono essere necessarie altre terapie quali la somministrazione di soluzione ipertonica o di vaptani (Tabella 2). Trattandosi di un’iponatremia transitoria a risoluzione spontanea, una singola somministrazione di Tolvaptan è in genere sufficiente. Recenti studi hanno mostrato come i vaptani rappresentino un trattamento efficace, sebbene siano gravati da un maggiore rischio di ipercorrezione [6]. Tuttavia, non sono stati riportati casi di mielinolisi pontina o altri effetti collaterali, probabilmente in virtù dell’esordio acuto dell’iponatremia. Il monitoraggio degli elettroliti e del bilancio idrico è fondamentale per decidere quando sospendere il trattamento, soprattutto qualora il paziente evolva verso una fase di AVP-D (trifasico), e per individuare casi di ipercorrezione che necessitino della somministrazione di fluidi ipotonici (Tabella 2).
L’iponatremia tardiva rappresenta la principale causa di ri-ospedalizzazione nei pazienti dimessi. Numerosi studi hanno dimostrato come la prescrizione di restrizione idrica preventiva alla dimissione sia in grado di ridurre l’incidenza di questa complicanza, la necessità di ri-ospedalizzazione ed i relativi costi, e sempre più centri si stanno uniformando a questa prescrizione in via profilattica [2].
TABELLA 1. Diagnosi differenziale della iponatremia dopo chirurgia della regione ipotalamo-ipofisaria
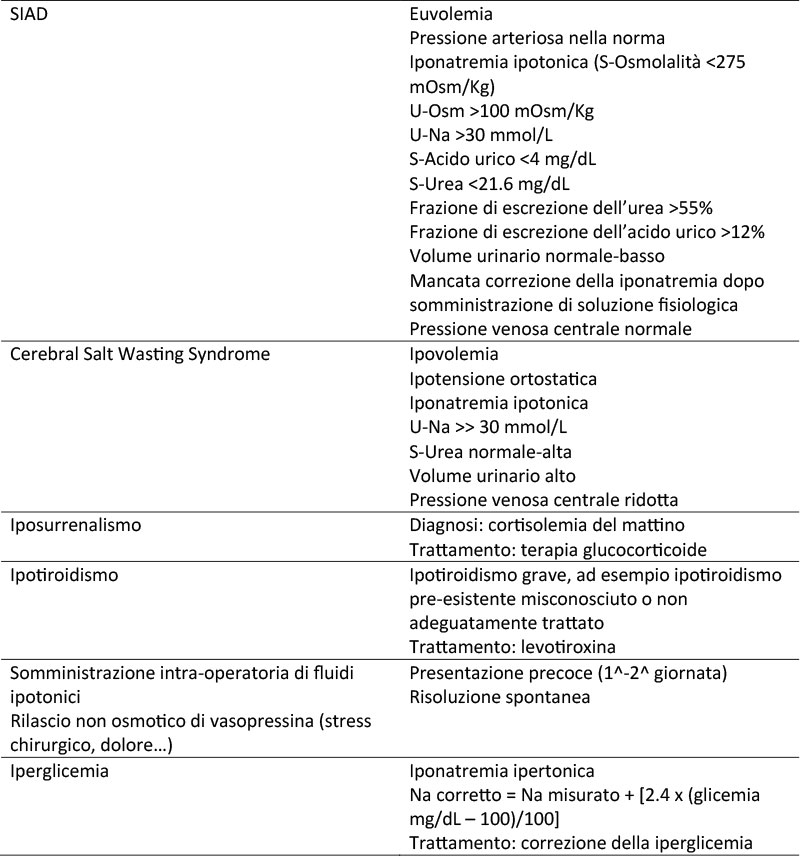
SIAD: sindrome da inappropriata antidiuresi
S-: sierico
U-: urinario
Na: sodio
Osm: osmolalità
TABELLA 2. Terapia della iponatremia ipotonica da sindrome da inappropriata antidiuresi (SIAD) dopo chirurgia ipotalamo-ipofisaria
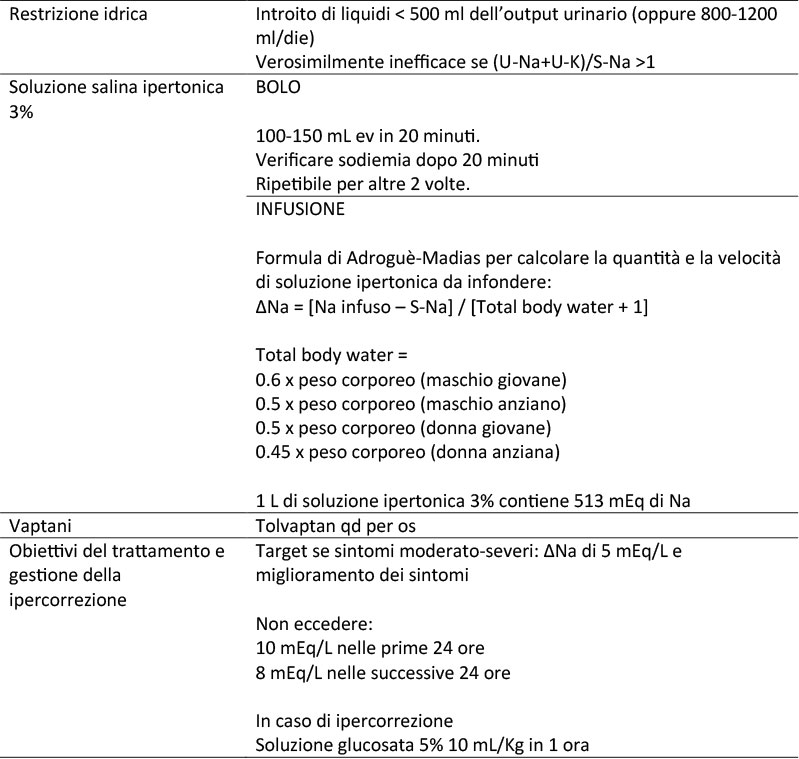
S-: sierico
U-: urinario
Na: sodio
K: potassio
Δ: variazione
Conflitto di interesse Gli autori dichiarano di non avere conflitti di interesse.
Consenso informato Lo studio presentato in questo articolo non ha richiesto sperimentazione umana.
Studi sugli animali Gli autori di questo articolo non hanno eseguito studi sugli animali
Riferimenti bibliografici
- Ferrante E, de Carvalho JF (2023) Syndrome of Inappropriate Antidiuresis. In: Caprio M, Fernandes-Rosa FL (a c di) Hydro Saline Metabolism: Epidemiology, Genetics, Pathophysiology, Diagnosis and Treatment. Springer International Publishing, Cham, pp 159–190
- Yuen KCJ, Ajmal A, Correa R, Little AS (2019) Sodium Perturbations After Pituitary Surgery. Neurosurg Clin N Am 30:515–524. https://doi.org/10.1016/j.nec.2019.05.011
- Woodmansee WW, Carmichael J, Kelly D, et al (2015) AMERICAN ASSOCIATION OF CLINICAL ENDOCRINOLOGISTS AND AMERICAN COLLEGE OF ENDOCRINOLOGY DISEASE STATE CLINICAL REVIEW: POSTOPERATIVE MANAGEMENT FOLLOWING PITUITARY SURGERY. Endocr Pract Off J Am Coll Endocrinol Am Assoc Clin Endocrinol 21:832–838. https://doi.org/10.4158/EP14541.DSCR
- Zada G, Liu CY, Fishback D, et al (2007) Recognition and management of delayed hyponatremia following transsphenoidal pituitary surgery. J Neurosurg 106:66–71. https://doi.org/10.3171/jns.2007.106.1.66
- Spasovski G, Vanholder R, Allolio B, et al (2014) Clinical practice guideline on diagnosis and treatment of hyponatraemia. Eur J Endocrinol 170:G1-47. https://doi.org/10.1530/EJE-13-1020
- Indirli R, Ferreira de Carvalho J, Cremaschi A, et al (2021) Tolvaptan in the Management of Acute Euvolemic Hyponatremia After Transsphenoidal Surgery: A Retrospective Single-Center Analysis. Front Endocrinol 12:689887. https://doi.org/10.3389/fendo.2021.689887
Scarica Articolo PDF



