L’ipofosfatemia (anche nota come ipofosforemia) è quella condizione caratterizzata da livelli ematici di fosforo inferiori a 2 .5 m g/dl (0.81 mmol/L). Si tratta di un disturbo raro nella popolazione generale, ma che possiamo osservare fino al 5% dei pazienti ospedalizzati. L'incidenza dell’ipofosfatemia acuta può però raggiungere anche valori più elevata, attestandosi intorno al 30-50% in specifici contesti ospedalieri quali le unità di terapia intensiva o in particolari condizioni cliniche quali l'alcolismo e gli stati settici (1).
L'ipofosfatemia può verificarsi per uno o più di tre meccanismi fisiopatologici principali:
a) ridoto assorbimento intestinale
b) eccessiva escrezione a livello renale
c) rapida redistribuzione dal liquido extracellulare al comparto intracellulare (shift transcellulare) (tabella 1).
Tabella 1. Cause di ipofosfatemia suddivise per meccanismo fisiopatologico
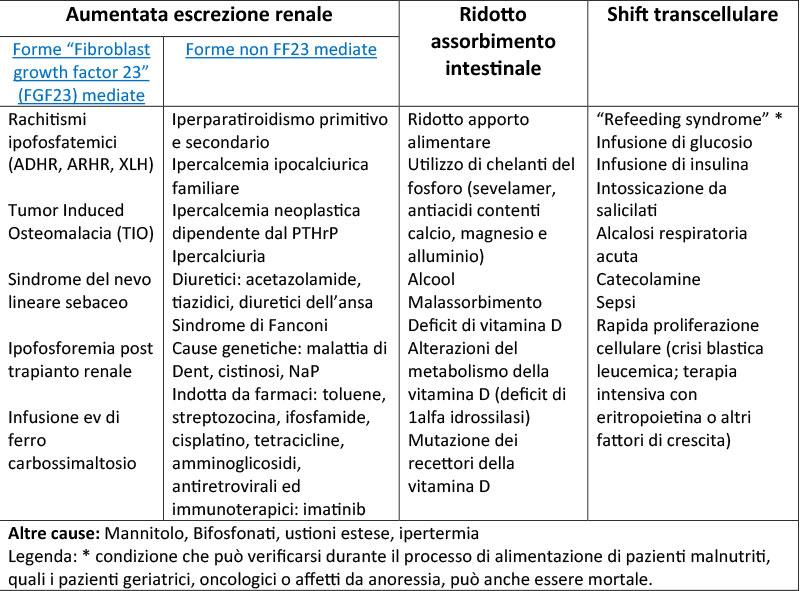
L'ipofosfatemia cronica riflette generalmente una condizione persistente di perdita del fosfato a livello tubulare renale. Tra le cause più comuni di ipofosfatemia renale abbiamo un'eccessiva attivazione dei recettori del paratormone PTH nel tubulo prossimale dovuta a iperparatiroidismo primitivo o secondario a deficit di vitamina D. Esistono poi malattie genetiche e acquisite che determinano una perdita tubulare di fosfato indipendente dal PTH. La causa più comune è l'ipofosfatemia X linked, dove una mutazione inattivante del gene PHEX determina un'aumentata espressione di Fibroblast growth factor 23(FGF23). Il quadro clinico tipico è caratterizzato da rachitismo con ipofosforemia, livelli di vitamina D inappropriatamente bassi o normali e ridotto riassorbimento tubulare dei fosfati. L’osteomalacia tumore indotta TIO è una malattia acquisita in cui un tumore di origine mesenchimale (generalmente benigno) secerne FGF3 o altre fosfatonine che determinano perdita urinaria di fosfati (2)
Dal momento che il fosfato è abbondante nei cibi, un inadeguato assorbimento intestinale non si osserva quasi più. Tuttavia, il digiuno o la denutrizione prolungata possono determinare una deplezione di fosfato e predisporre ad una successiva ipofosfatemia durante la ripresa dell'alimentazione soprattutto se accompagnate da infusioni endovenose di glucosio (
shift transcellulare).
L'ipofosfatemia si distingue in: lieve (2-2.5 mg/dl); moderata (1-1.9 mg/dL) e severa (<1 mg/dl).
L'ipofosfatemia è generalmente asintomatica fino a quando la concentrazione ematica di fosforo non scende al di sotto di 0.8-1.2 mg/dl. Le manifestazioni cliniche dell'ipofosfatemia dipendono dall'entità e dalla durata della deplezione dei fosfati.
La sintomatologia consiste inizialmente in astenia, debolezza muscolare e anoressia. Nelle forme croniche la presentazione clinica molto sfumata, caratterizzata da sintomi muscoloscheletrici; talvolta il primo segno clinico è rappresentato da un evento fratturativo nell'ambito di un quadro di osteomalacia misconosciuta (1).
In caso di ipofosfatemia severa/acuta (<1.5 mg/dL) invece la clinica consiste in grave miopatia, rabdomiolisi, fratture multiple, cardiomiopatia, aritmia, encefalopatia e gravi deficit neuromuscolari che possono culminare nel coma fino alla morte.
Diagnosi
Nella valutazione iniziale, oltre ai livelli di fosforo vanno valutati contemporaneamente i livelli di calcio totale, calcio ionizzato, PTH e 25 OH vitamina D nonché la calciuria e la fosfaturia delle 24 ore, dal momento che i livelli di fosforo i solati non sono indicatori del contenuto totale di fosfati dell'organismo (3). Il primo step nell'algoritmo diagnostico consiste nel distinguere le forme renali da quelle non renali (Fig.1)
Figura1. Algoritmo diagnostico dell'ipofosfatemia
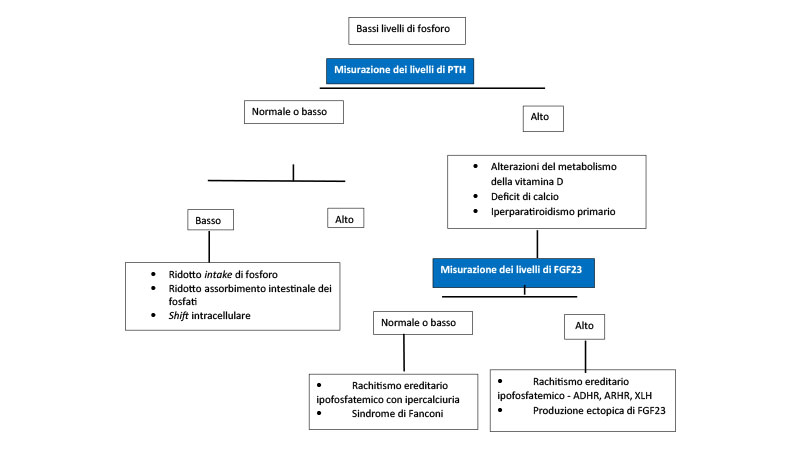
L'escrezione urinaria di fosfato può essere valutata mediante la fosfaturia delle 24 ore, con calcolo della frazione di escrezione del fosforo (FEp) e la determinazione del riassorbimento tubulare massimo dei fosfati (RTP) corretto per il filtrato glomerulare (TmP/GFR).
La frazione di escrezione del fosforo si calcola nel seguente modo: FEP=1- [(fosforo urine /fosforo plasma) x (creatinina pl
asm
a / creatinina urin
e; mentre il riassorbimento tubulare dei fosfati può essere calcolato come RTP= 1-FEP.
Se RTP è ≤ 0.85, la relazione tra fosfatemia e fosfaturia è lineare e l'algoritmo fornisce già il valore reale del TmP/GFR (TmP/GFR = RTP x fosfatemia). Se, invece, il RTP è >0.85, la relazione non è più lineare e deve essere utilizzata la seguente formula: TmP/GFR = (0.3 x RTP) / [1 - (0.8 x RTP)] x fosfatemia.
Laddove il TmP/GFR è basso (<2.1 mg/dL) si può attribuire l'ipofosfatemia ad un'eccessiva perdita renale di fosforo; in questo caso è utile il dosaggio di FGF23 che consente di differenziare tra le forme FGF23 mediate e quelle non mediate da FGF23(3).
Terapia
Il trattamento dell'ipofosfatemia dipende dalla causa, dalla durata e dalla severità del deficit e dalle comorbidità del paziente.
Le forme lieve e moderata possono essere trattate con aumento dell'intake alimentare di fosforo mediante supplementazioni orali; mentre le forme severe richiedono terapia con fosforo endovena. I Sali di fosfato più utilizzati nella pratica clinica sono il potassio fosfato e il sodio fosfato (4).
Nei pazienti che presentano concomitante ipokaliemia è preferibile usare supplemento di potassio fosfato; mentre in quelli con iperkaliemia e/o IRC, vi è indicazione ad utilizzare supplemento di sodio fosfato. Nei pazienti con sovraccarico di volume si raccomanda, quando possibile, di evitare supplemento di sodio fosfato.
Il fosforo endovena deve essere usato con cautela a causa del rischio di ipocalcemia acuta (soprattutto in caso di insufficienza renale cronica). Analogamente, nei pazienti iper/ipocalcemici (4) si raccomanda di evitare iperfosfatemia da ipercorrezione.
Infine, nelle forme renali FGF23-mediate bisogna effettuare la supplementazione oltre che con i fosfati anche con analoghi attivi della vitamina D come il calcitriolo.



