Guglielmo Beccuti1, Angelo Armandi2, Mirko Parasiliti Caprino1
1SC Endocrinologia, Diabetologia e Metabolismo U, Dipartimento di Scienze Mediche, Università degli studi di Torino, Torino, Italia
2SC Gastroenterologia U, Dipartimento di Scienze Mediche, Università degli studi di Torino, Torino, Italia
Autore corrispondente G. Beccuti [email protected]
Introduzione
Un importante avanzamento in ambito epatologico è rappresentato dall’introduzione del nuovo concetto di steatosi epatica associata a disfunzione metabolica (MAFLD) nel 2020 [1], in sostituzione della steatosi epatica non alcolica (NAFLD) risalente al 1986.
Il termine MAFLD, con cui la comunità endocrino-diabetologica è chiamata a confrontarsi, indica la presenza di steatosi epatica definita da tecniche di immagine (ecografia o risonanza magnetica del fegato) o dalla evidenza istologica di accumulo grasso intra-epatocitario superiore al 5%, dalla biopsia epatica associata a uno di questi elementi: 1) diabete mellito tipo 2 (DMT2); 2) eccesso ponderale; 3) la presenza di almeno due fattori di rischio metabolici: adiposità viscerale, ipertensione arteriosa, ipertrigliceridemia, HDL basso, alterata glicemia a digiuno, insulino-resistenza e incremento della proteina C reattiva (Fig. 1).
Vantaggi e limiti della nuova definizione
Il concetto di MAFLD introduce dei criteri diagnostici positivi, anziché di esclusione come nel caso della NAFLD, e include un gruppo eterogeneo di alterazioni epatiche che condividono la stessa eziopatogenesi metabolica. Inoltre, la nuova definizione supera la dicotomia istologica di steatoepatite non alcolica (NASH) versus accumulo semplice di grasso (NAFL), considerando piuttosto la MAFLD come un continuum di lesioni epatiche a gravità progressiva, al pari delle altre epatopatie croniche, con importanti implicazioni anche per i trial farmacologici. La severità della MALFD si basa sul livello di progressione fibrosa, che viene generalmente valutata in maniera non invasiva mediante sistemi di punteggio, di cui il fibrosis-4 (FIB-4) è il maggiormente validato [2], oppure tramite tecniche elastografiche.
Quando la MAFLD si associa ad altre malattie epatiche croniche (es. su base alcolica, virale, autoimmune, farmacologica, ecc.), si parla di malattia steatosica a eziologia multipla (Tab. 1). Seppur l’esclusione di altre epatopatie non sia un prerequisito per la diagnosi di MAFLD, esse andrebbero comunque indagate poiché possono contribuire a una prognosi peggiore.
La diagnosi di MAFLD, attraverso nuovi criteri di inclusione, si estende a un maggior numero di soggetti, tra cui quelli con alterazioni metaboliche associate a un aumento del rischio cardiovascolare e con altre epatopatie.
Un limite potrebbe essere rappresentato dall’eterogeneità con cui si definisce la presenza di steatosi, con conseguente variabilità fenotipica della MAFLD.
Steatosi epatica nel diabete mellito tipo 2
La prevalenza della steatosi raggiunge il 70-80% nel DMT2 e il 25-30% nella popolazione generale [3]; questa condizione si associa a un aumento del rischio di mortalità cardiovascolare e di complicanze sia epatiche che extraepatiche.
Un documento utile per l’inquadramento della steatosi nella medicina primaria e in ambito endocrinologico è rappresentato dalle linee guida (LG) dell’American Association of Clinical Endocrinology, in collaborazione con l’American Association for the Study of Liver Diseases [4]. Pur risalendo al 2022, le LG utilizzano i criteri di esclusione della NAFLD. Una volta definita la presenza di steatosi su base radiologica o istologica, le LG raccomandano lo screening delle condizioni a maggior rischio di evoluzione fibrotica, in particolare attraverso il test validato FIB-4, che richiede l’età del soggetto, i livelli di AST-ALT e la conta piastrinica.
Sulla base del punteggio del FIB-4, i soggetti a rischio intermedio necessitano di un ulteriore test non invasivo, che prevede in particolare la valutazione della stiffness (“durezza”) del fegato tramite elastografia. Dove disponibile, anche l’ELF (enhanced liver fibrosis) test, protetto da brevetto, può essere utilizzato, con accuratezza comparabile all’elastografia. I soggetti a rischio intermedio con steatosi all’imaging o aumentati livelli di ALT o AST e i soggetti a rischio elevato richiedono un inquadramento multidisciplinare che includa una valutazione epatologica.
Terapie antidiabetiche
Le LG affermano che metformina, acarbosio, DPP4-inibitori e insulina non sono raccomandati per il trattamento della steatoepatite, in quanto privi di benefici sulla necrosi epatocitaria o sull’infiammazione, ma la loro assunzione come farmaci antidiabetici può proseguire se necessario.
Il pioglitazone e i GLP-1 RA (in particolare liraglutide e semaglutide) sono raccomandati nel DMT2 in presenza di steatoepatite documentata e dovrebbero essere presi in considerazione in caso di aumentato rischio di steatoepatite sulla base di test non invasivi o degli aumentati livelli di transaminasi (raccomandazione grado A). Dati meta-analitici evidenziano un effetto dei GLP-1 RA sulla riduzione del contenuto di grasso intraepatico e sulla regressione dell’infiammazione all’esame istologico [5].
La classe degli SGLT2i non esercita effetti significativi sull’attività di malattia, seppur si associ a una riduzione del grasso intraepatico [6].
Conclusioni
La MAFLD è considerata oggigiorno un “barometro della salute metabolica”, con un ruolo chiave per l’endocrinologo-diabetologo nell’identificazione precoce di questa condizione e della progressione di malattia, nonché nella gestione multidisciplinare e nel trattamento del DMT2 con farmaci raccomandati.
Figura 1. Criteri diagnostici della steatosi epatica associata a disfunzione metabolica (MAFLD)
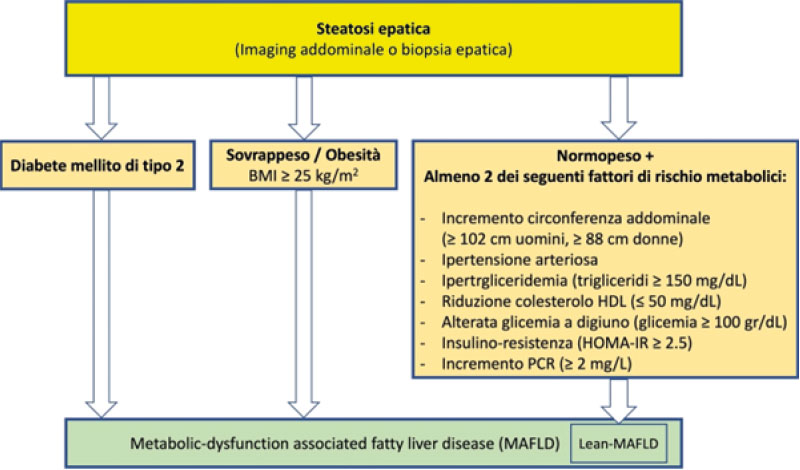 Tabella1
Tabella1 Malattia steatosica a eziologia multipla




