Gestione ambulatoriale del paziente con iponatremia ipotonica cronica
Nunzia Prencipe, Andrea Benso, Emanuele Varaldo, Alessandro Maria Berton
S.C. Endocrinologia, Diabetologia e Metabolismo U., A.O.U. Città della Salute e della Scienza di Torino, Dipartimento di Scienze Mediche, Università degli Studi di Torino, Torino, Italia
Autore corrispondente Nunzia Prencipe nunzia.prencipe@gmail.com
Introduzione
L'iponatremia (IpoNa) è l’alterazione elettrolitica più comune nella pratica clinica, e in particolare la forma ipotonica può risultare severamente sintomatica 1,2. Se l’IpoNa acuta (< 48h) spaventa per il corredo di sintomi moderati o severi a cui si associa, quella cronica (> 48h) viene frequentemente trascurata, poiché considerata asintomatica e di scarso impatto clinico, mentre comporta a sua volta una maggior incidenza di disturbi cognitivi, della marcia, cadute e osteoporosi 1,3,4. La differente sintomatologia è data dal tempo a disposizione dei neuroni per mettere in atto meccanismi di compenso all’ipotonicità protratta; i quali espongono d’altro canto a un maggior rischio di mielinolisi pontina in caso di ipercorrezione. Se non possibile stimare con sicurezza il tempo di insorgenza, tutte le IpoNa di primo riscontro sono pertanto da considerarsi croniche5,6.
Inquadramento clinico
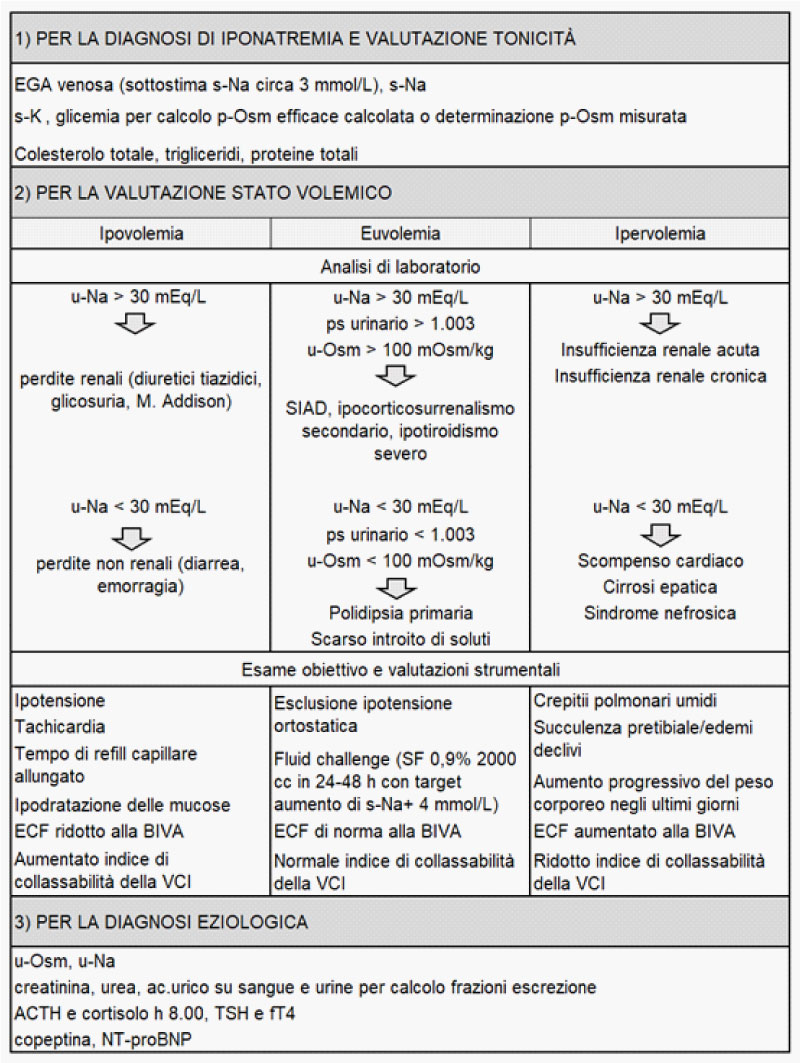
Risulta necessario 1,3,5,6: 1) confermare il dato laboratoristico e definire la tonicità plasmatica; 2) trovare indizi relativi allo stato volemico del paziente e 3) identificare l’eziopatogenesi della disionia. A tal fine, sono impiegabili esami biochimici e strumentali di supporto, ma non di meno un accurato esame obiettivo e approfondita indagine anamnestica (Tab 1).
Trattamento
Le forme ipervolemiche e francamente ipovolemiche risultano più facilmente diagnosticabili. In questo caso il trattamento è strettamente correlato alla patologia di fondo e si basa sul ripristino del fisiologico volume extracellulare 1,5,6. Nei casi euvolemici e soprattutto nella sindrome da inappropriata antidiuresi (SIAD), invece, non solo la diagnosi è più complessa, ma spesso la causa scatenante non è chiara e/o non modificabile. In questo caso entrano in gioco trattamenti farmacologici e non, con lo scopo di aumentare l’escrezione di acqua libera da elettroliti 5,6.
La restrizione idrica, quando possibile, è l’opzione terapeutica di prima linea, in considerazione del razionale fisiopatologico e del basso rischio di ipercorrezione. Si raccomanda di ridurre l’introito idrico di almeno 500 cc rispetto all’output urinario e, per stimarne la probabilità di efficacia, è d’aiuto l’indice di Furst [(u-K + u-Na spot) /s-Na] con valori > 1 indicativi di scarsa risposta). La restrizione idrica è controindicata in condizioni a rischio di severa disidratazione e/o vasospasmo cerebrale ed inoltre spesso mal tollerata se < 1000 cc/die.
Una strategia complementare, in particolare nei pazienti anziani e sarcopenici, è garantire un adeguato apporto di soluti con la dieta per favorire l’acquaresi, attraverso un approccio multidisciplinare e nutrizionale di supporto.
L’urea agisce come diuretico osmotico, è filtrata liberamente dal glomerulo e rappresenta il 50% del carico osmotico quotidiano eliminato con l’urina, mentre costituisce solo il 2% dei soluti plasmatici. Si stima che 30 g di urea (corrispondenti a circa 500 mOsm) siano in grado di eliminare con le urine circa 1000 cc di acqua libera. La dose utilizzata è di 15-90 g/die (in media 30-45 g/die). Sebbene rappresenti una terapia efficace, è spesso poco tollerata per la scarsa palatabilità e non risulta attualmente rimborsabile dal Sistema Sanitario Nazionale italiano.
Tolvaptan, antagonista selettivo del recettore V2 per la vasopressina con azione acquaretica, è l’unico farmaco attualmente rimborsato in Italia per il trattamento della SIAD. È indicato solo nei pazienti con natremia moderata-severa (120-129 mmol/L) paucisintomatica. La dose di partenza consigliata è 15 mg (7.5 mg in soggetti fragili), ma la prima assunzione richiede l’ospedalizzazione del paziente per necessità di uno stretto monitoraggio dei valori di sodio a fronte del rischio di ipercorrezione. Pertanto, nel contesto ambulatoriale non sempre è un trattamento percorribile nell’immediato e potrebbe essere necessaria una terapia alternativa “ponte”.
Empagliflozin, per il meccanismo di azione glicosurico, potrebbe risultare una terapia valida, almeno di associazione, sia per le forme ipervolemiche che per la SIAD. In tale ambito sono però ancora pochi gli studi di efficacia ed al momento è indicato solo in pazienti diabetici o con scompenso cardiaco.
Conclusioni
L’armamentario a disposizione del clinico per la gestione ambulatoriale del paziente iponatremico cronico è vario (Tab. 2), ma ogni trattamento presenta vantaggi e svantaggi che devono essere attentamente analizzati e condivisi con il paziente in base al quadro di salute globale, alle preferenze personali, alle disponibilità economiche e alla possibilità di ricovero. A prescindere dall’atteggiamento terapeutico adottato, questi pazienti, richiedono un iniziale monitoraggio biochimico e clinico stretto, almeno fino a stabilizzazione del quadro patologico di base e dei valori di natremia. É, inoltre, utile fornire indicazioni al Curante circa l’introito idrico quotidiano suggerito e i trattamenti da evitare, in quanto in grado di favorire l’attività del sistema antidiuretico (ad es. diuretici tiazidici, FANS, SSRI, oppiacei, etc.).
Tabella 1. Valutazioni cliniche, biochimiche e strumentali per l'inquadramento dell'iponatremia
Leggenda: ECF: extracellular fluid; BIVA: Bioelectrical Impedance Vector Analysis; VCI: vena cava inferiore
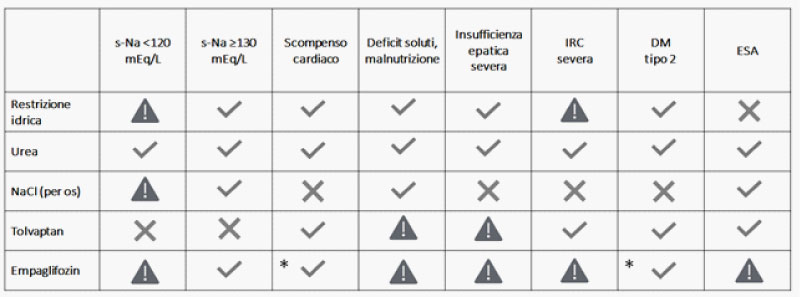
Tabella 2. Terapie a disposizione del clinico per la gestione ambulatoriale del paziente iponatremico cronico.
LEGENDA:
 *L’asterisco indica le patologie per cui il farmaco ha attualmente l’indicazione in scheda tecnica.
*L’asterisco indica le patologie per cui il farmaco ha attualmente l’indicazione in scheda tecnica.
IRC = insufficienza renale cronica; DM = diabete mellito; ESA = emorragia sub-aracnoidea
Conflitti di interesse Gli autori dichiarano di non avere conflitti di interesse
Consenso informato Lo studio presentato in questo articolo non ha richiesto sperimentazione umana.
Studi sugli animali Gli autori di questo articolo non hanno eseguito studi sugli animali
Riferimenti bibliografici
- Adrogué HJ, Tucker BM, Madias NE. Diagnosis and Management of Hyponatremia: A Review. JAMA. 2022;328(3):280-291. doi:10.1001/jama.2022.11176
- Schrier RW, Sharma S, Shchekochikhin D. Hyponatraemia: more than just a marker of disease severity? Nat Rev Nephrol. 2013;9(1):37-50. doi:10.1038/nrneph.2012.246
- Sbardella E, Isidori AM, Arnaldi G, et al. Approach to hyponatremia according to the clinical setting: Consensus statement from the Italian Society of Endocrinology (SIE), Italian Society of Nephrology (SIN), and Italian Association of Medical Oncology (AIOM). J Endocrinol Invest. 2018;41(1):3-19. doi:10.1007/s40618-017-0776-x
- Williams DM, Gallagher M, Handley J, Stephens JW. The clinical management of hyponatraemia. Postgraduate Medical Journal. Published online April 4, 2016:postgradmedj-2015-133740. doi:10.1136/postgradmedj-2015-133740
- Spasovski G, Vanholder R, Allolio B, et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia. Eur J Endocrinol. 2014;170(3):G1-47. doi:10.1530/EJE-13-1020
- Verbalis JG, Goldsmith SR, Greenberg A, et al. Diagnosis, Evaluation, and Treatment of Hyponatremia: Expert Panel Recommendations. The American Journal of Medicine. 2013;126(10):S1-S42. doi:10.1016/j.amjmed.2013.07.006
Scarica Articolo PDF